Leuckartova reakce
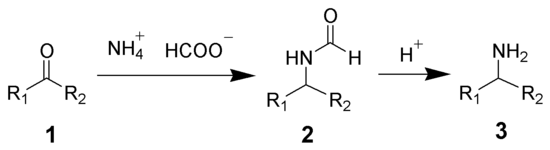
Leuckartova reakce je organická reakce, při které se mění aldehydy či ketony na aminy prostřednictvím reduktivní aminace při zahřívání reakční směsi.[1][2] Používá se při ní mravenčan amonný nebo formamid, jako zdroj dusíku a redukční činidlo.[3]
K této reakci jsou potřeba vysoké teploty, obvykle mezi 120 a 130 °C; při použití formamidu i nad 165 °C.[1]
Historie[editovat | editovat zdroj]
Leuckartova reakce je pojmenována po německém chemikovi Rudolfu Leuckartovi, který zjistil, že zahříváním benzaldehydu s formamidem nevzniká předpokládaný benzylidendiformamid, nýbrž fenylmethylamin.[4]
V roce 1891 jeho spolupracovník Otto Wallach provedl další reakce aldehydů a alicyklických a terpenoidových ketonů, čímž poukázal na obecnou využitelnost reakce.[4] Postupně bylo nalezeno několik způsobů, jak zlepšit výtěžnost reakce a uskutečnit ji za mírnějších podmínek. C. B. Pollard a David C. Young prověřili několik způsobů tvorby aminů: použití formamidu, mravenčanu ammonného nebo obou těchto látek, případně přidání kyseliny mravenčí k formamidu;[3] nejlepší výsledky byly při použití samotného mravenčanu.[1][3] U formamidu byly výtěžky nižší, ovšem šlo je zvýšit použitím velkého přebytku formamidu nebo přidáním mravenčanu amonného, síranu amonného, nebo chloridu hořečnatého jako katalyzátoru.[5]
Mechanismus[editovat | editovat zdroj]
S mravenčanem amonným[editovat | editovat zdroj]

Mravenčan amonný se nejprve disociuje na kyselinu mravenčí a amoniak, amoniak poté nukleofilně atakuje karbonylový uhlík.[3] Kyslík deprotonuje dusík a vytvoří hydroxyl. Hydroxyl se poté protonuje vodíkem z kyseliny mravenčí, čímž vzniká molekula vody a rezonančně stabilizovaný karbokation. Ten následně reaguje s vodíkem pocházejícím z kyseliny mravenčí a vytvoří se oxid uhličitý a amin.
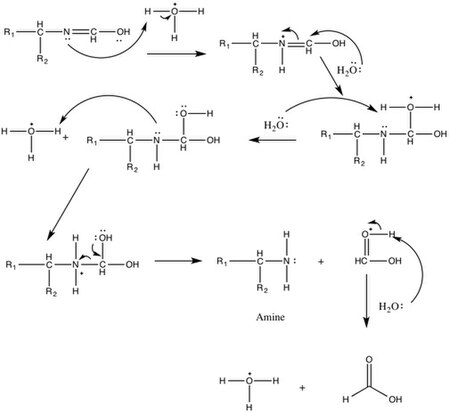
S formamidem[editovat | editovat zdroj]

Formamid nukleofilně atakuje karbonylový uhlík,[3] poté je kyslík protonován odštěpením vodíkového atomu od dusíku, což vytvoří vodu a rezonančně stabilizovaný N-formylový meziprodukt.[3] Voda hydrolyzuje formamid na mravenčan amonný, jenž slouží jako aktivní redukční činidlo a váže se na N-formylovou sloučeninu. Proběhne přenos hydridu, který způsobí oddělení oxidu uhličitého. Amonný kation vytvoří imin a uvolní amoniak. Imin je nakonec hydrolyzován za tvorby aminu.
Použití[editovat | editovat zdroj]
Leuckartova reakce je součástí syntézy tetrahydro-1,4 benzodiazepin-5-onu, molekuly patřící mezi benzodiazepiny.[6]
Mnoho těchto sloučenin potlačuje činnost centrální nervové soustavy a využití mají například v antibiotikách a při léčbě vředů a HIV.[6] Tetrahydro-1,4-benzodiazepin-5-ony lze s využitím Leuckartových reakcí připravit s vysokými výtěžky a velmi čisté; jako redukční činidlo při tom slouží kyselina mravenčí.[6]
Odkazy[editovat | editovat zdroj]
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Leuckart reaction na anglické Wikipedii.
- ↑ a b c Elliot Alexander; Ruth Bowman Wildman. Studies on the Mechanism of the Leuckart Reaction. Journal of the American Chemical Society. 1948, s. 1187–1189. DOI 10.1021/ja01183a091. PMID 18909189.
- ↑ A. W. Ingersoll. α-Phenylethylamine. Organic Syntheses. 1937, s. 76. DOI 10.15227/orgsyn.017.0076.
- ↑ a b c d e f C. B. Pollard; David C. Young. The Mechanism of the Leuckart Reaction. Journal of Organic Chemistry. 1951, s. 661–672. DOI 10.1021/jo01145a001.
- ↑ a b Frank S. Crossley; Maurice L. Moore. Studies on the Leuckart Reaction. Journal of Organic Chemistry. 1944, s. 529–536. DOI 10.1021/jo01188a006.
- ↑ Vincent J. Webers; William F. Bruce. The Leuckart Reaction: A study of the Mechanism. Journal of the American Chemical Society. 1948, s. 1422–1424. DOI 10.1021/ja01184a038. PMID 18915755.
- ↑ a b c Sung-Chan Lee; Seung Bum Park. Novel application of Leuckart–Wallach reaction for synthesis of tetrahydro-1,4-benzodiazepin-5-ones library. Chemical Communications. 2007, s. 3714–3716. Dostupné online. DOI 10.1039/B709768A. PMID 17851604.
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Leuckartova reakce na Wikimedia Commons
Obrázky, zvuky či videa k tématu Leuckartova reakce na Wikimedia Commons
