Klatrát

Klatrát je chemická látka skládající se z matrice tvořené jednou sloučeninou (hostitelskou), která zachycuje nebo obsahuje molekuly jiné sloučeniny (hostující). Slovo klatrát je odvozeno z latinského clathratus, což znamená „s mřížemi“. Většina klatrátových sloučenin je polymerních a zcela obaluje hostující molekulu.[2] Podle IUPAC jsou klatráty inkluzní sloučeniny, "ve kterých je hostující molekula v kleci tvořené hostitelskou molekulou nebo matricí hostitelských molekul." Termín zahrnuje mnoho molekulárních hostitelů, včetně kalixarenů a cyklodextrinů a dokonce i některých anorganických polymerů, jako jsou zeolity.
Klatráty lze rozdělit na klatrátové hydráty, anorganické klatráty a organické klatráty. Každý klatrát se skládá z matrice hostitelských molekul, která obsahuje dutiny (klece), a hostujících molekul, které jsou v dutinách matrice zachyceny.
Dva nejběžnější typy klatrátových matric jsou označovány typ I (sI) a typ II (sII). Molární podíl molekul matrice v těchto klatrátech je asi 85 %:
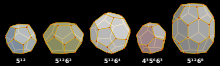
- elementární buňku matrice typu I tvoří 46 hostitelských molekul uspořádaných do dvou typů klecí – dvou malých dvanáctistěnných složených z pětiúhelníků (označovaných 512) a šesti velkých čtrnáctistěnných složených z dvanácti pětiúhelníků a dvou šestiúhelníků (512 62), v nichž je uzavřeno celkem 8 hostujících molekul; na jednu hostující molekulu připadá 5,75 hostitelské molekuly (46 molekul matrice na 8 hostujících molekul, tj. molární podíl 85,2 %),
- u typu II je elementární buňka matrice tvořena 136 molekulami (16 malých klecí 512 a 8 velkých šestnáctistěnných klecí 512 64; na jednu hostující molekulu připadá 52⁄3 hostitelské molekuly (136:24, tj. molární podíl 85 %).
Matrice klatrátových hydrátů je tvořena molekulami vody, které se "samoasociují" prostřednictvím vodíkových vazeb. Malé (tzv. hostující) molekuly (metan, oxid uhličitý, vodík) jsou pak v hydrátech zachyceny. Interakce hosta s hostitelem je omezena na Van der Waalsovy síly. Určité výjimky existují v semiklatrátech, kde se hostující molekuly začleňují do hostitelské matrice prostřednictvím vodíkových vazeb s hostitelskými molekulami. Při nižším podílu hostujících molekul se matrice částečně zhroutí na některou krystalovou strukturu ledu. Klatrátové hydráty jsou stabilní při nízkých teplotách a vysokém tlaku a mají podobné vlastnosti jako led (například elektrický odpor), jejich teplota tání je však o několik °C vyšší.[3] Klatrátové hydráty se přirozeně vyskytují v permafrostu a oceánských sedimentech.
Matrice anorganických klatrátů je vázána kovalentně, hosty jsou typicky alkalické kovy nebo kovy alkalických zemin. Díky silnější kovalentní vazbě jsou klece obvykle menší než u klatrátových hydrátů. Hostující atomy interagují s hostitelem iontovými nebo kovalentními vazbami. Většina stabilních anorganických klatrátů má klece plně obsazené hostujícími atomy. Anorganické klatráty mohou být syntetizovány přímou reakcí v kulovém mlýně při vysokých teplotách nebo krystalizací z taveniny. Vzhledem k rozmanitosti hostitelských a hostujících prvků jsou anorganické klatráty chemicky mnohem rozmanitější než klatrátové hydráty a mají širokou škálu vlastností. Nejpozoruhodnější je, že mezi anorganickými klatráty lze nalézt jak izolanty, tak i supravodiče (Ba8Si46). Společnou vlastností anorganických klatrátů, která vědce zaujala, je nízká tepelná vodivost. Ta je přisuzována schopnosti hostujícího atomu "vibrovat" v rámci hostitelské struktury, což rozptyluje fonony, které přenášejí teplo.[1]
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Clathrate compound na anglické Wikipedii.
- ↑ a b c KRISHNA, Lakshmi; KOH, Carolyn A. Inorganic and methane clathrates: Versatility of guest–host compounds for energy harvesting. S. 8. MRS Energy & Sustainability [online]. Springer Nature, 2015-08-28 [cit. 2024-05-04]. Roč. 2, čís. 1, s. 8. Dostupné online. ISSN 2329-2237. DOI 10.1557/mre.2015.9. (anglicky)
- ↑ ATWOOD, Jerry L. Inclusion Compounds. Ullmann's Encyclopedia of Industrial Chemistry [online]. Wiley, 2003-03-11 [cit. 2024-05-04]. Dostupné online. DOI 10.1002/14356007.a14_119. (anglicky)
- ↑ HRNČÍŘ, Matěj. Návrh nové experimentální trati pro výrobu hydrátů CO2 pro možné využití v energetice. Praha, 2023 [cit. 2024-05-04]. 99 s. Diplomová práce. ČVUT, Fakulta strojní. Vedoucí práce Ing. Ondřej Bartoš, Ph.D.. Dostupné online.
